LES ESPECES MINERALES
I) Introduction.
Les minéraux, solides naturels cristallins, sont des constituants des matériaux terrestres mais aussi des planètes du système solaire. L’étude des minéraux est la minéralogie. Les minéraux (le mot vient de mine) sont le plus souvent de cristaux dont l’étude individuelle est la cristallographie.
Un cristal est un solide macroscopiquement homogène, ordonné à l’échelle atomique et défini par une composition chimique donnée.
Un minéral est un cristal existant dans la nature, caractérisé fréquemment à l’œil par des faces géométriques régulières s’il a pu croître dans son milieu naturel.
Un minerai est un minéral ou un ensemble rocheux contenant un ou des minéraux utiles à l’Homme. En pratique, le terme s’applique surtout aux minerais métalliques.
La plupart des minéraux sont des solutions solides ou des cristaux mixtes.
90% des roches sont constituées de silicates (c'est-à-dire contenant de la silice SiO2).Les minéraux non silicatés ne représentent que 5% des solides constituant la croûte terrestre mais leur importance peut être grande d’un point de vue économique : ils sont en général plus facile à exploiter industriellement que les silicates.
A coté des éléments natifs, c'est-à-dire qui se rencontrent dans la nature à l’état pur, comme l’or, l’argent, le cuivre, le soufre, le carbone pur (diamant et graphite), les principaux groupes sont : les halogénures (chlorures, fluorures), les sulfures, les oxydes, les carbonates, principalement formés dans les milieux marins (calcite), les sulfates (dont le gypse ou pierre à plâtre), les phosphates.
II) Caractéristiques et propriétés des minéraux
1) La forme (les 7 systèmes cristallins)
Les formes cristallines et les symétries qui en découlent ont fait regrouper les cristaux en 7 systèmes cristallographiques (appelés systèmes cristallins). Cela se retrouve en observant la régularité des faces et leur symétrie avec le coté opposé. En effet, si une face est visible sur un coté du cristal, il en existe obligatoirement une autre symétrique sur le coté opposé (sur des agrégats, il est très difficile de montrer cette symétrie, les faces des cristaux étant trop enchevêtrées).
L'arrangement des atomes est défini dans la maille élémentaire (plus petit arrangement définissant le réseau cristallin), le cristal est une juxtaposition d'une multitude de mailles élémentaires.
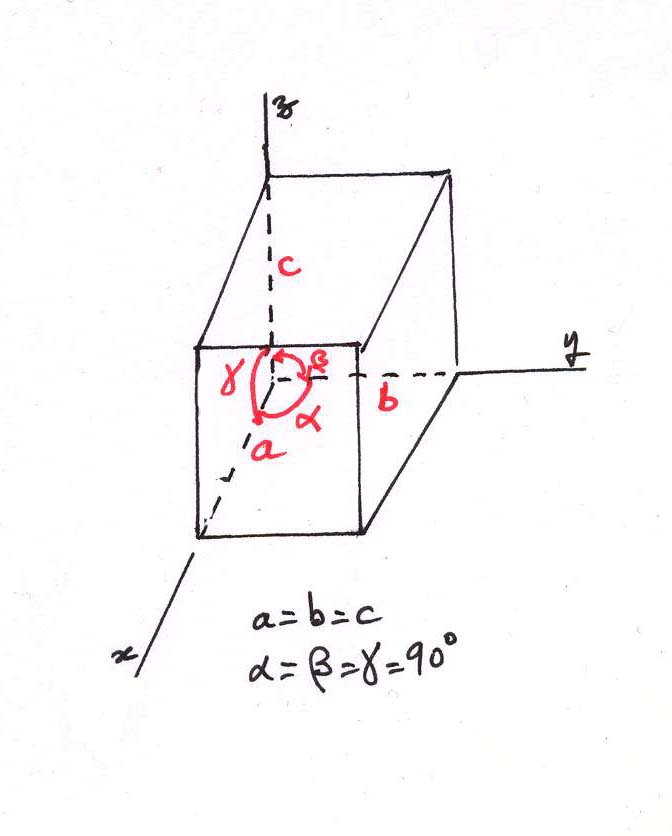
-le système cubique :
La maille élémentaire a la forme d'un cube. La pyrite de fer et le grenat sont classés dans ce système.

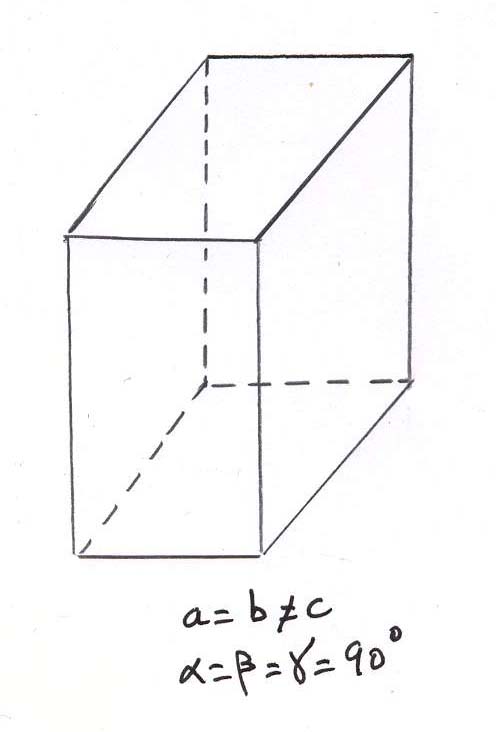
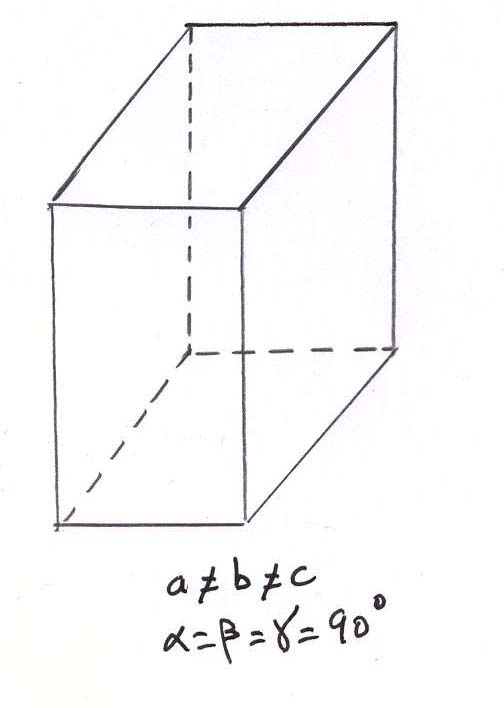
-le système quadratique :
La maille élémentaire est un prisme droit à base carrée. Le zircon, la wulfénite et la vésuvianite cristallisent dans ce système.
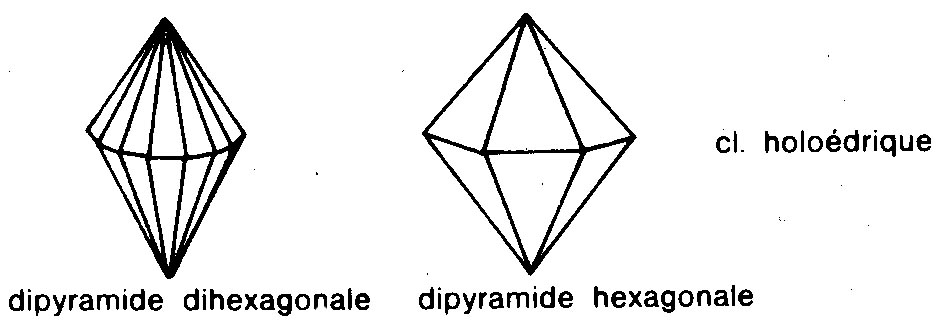
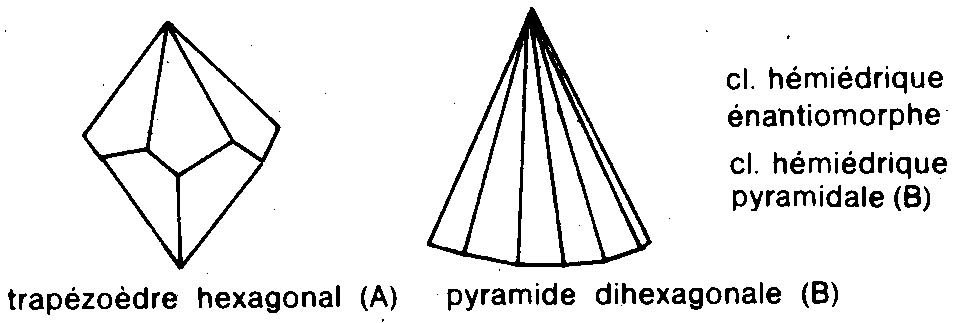
- le système hexagonal :
La maille élémentaire est un prisme droit à base hexagonale (six faces). Le béryl (émeraude de Colombie), l’apatite et la glace cristallisent dans ce système. La référence à la glace permet de réaliser le nombre important de cristaux différents qui peuvent être construits dans un système donné, ce qui n’empêche pas chaque cristal de flocon de neige d’avoir l’air unique.

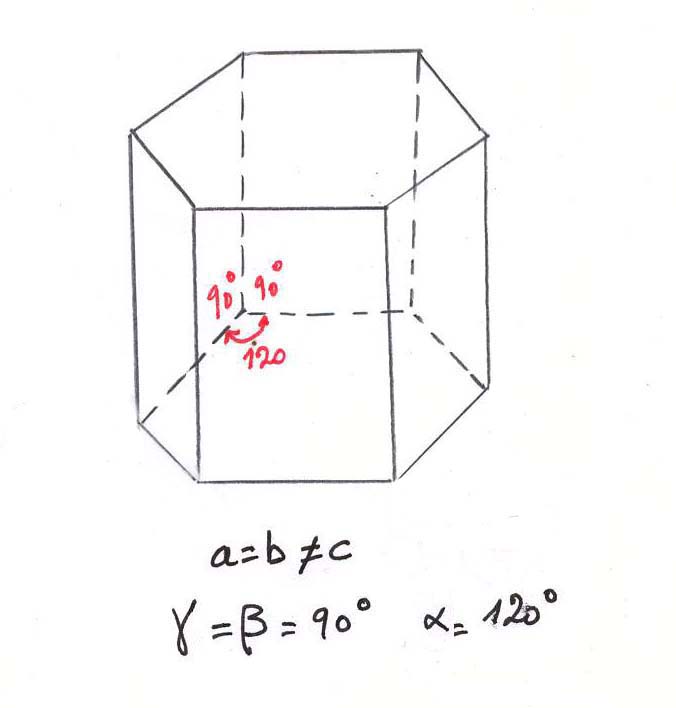
-le système rhomboédrique :
La maille élémentaire est le rhomboèdre: parallélépipède dont les six faces sont des losanges. Le quartz, la tourmaline, le corindon, la sidérite et la calcite appartiennent au même système rhomboédrique.
Il y a plus de 300 formes différentes de cristallisation de la calcite.
Le quartz cristallise à basse température dans un système rhomboédrique (filons) et à haute température dans un système hexagonal (métamorphisme, comme le quartz cristallise en dernier, il occupe les interstices disponibles et il n'a pas de forme propre).
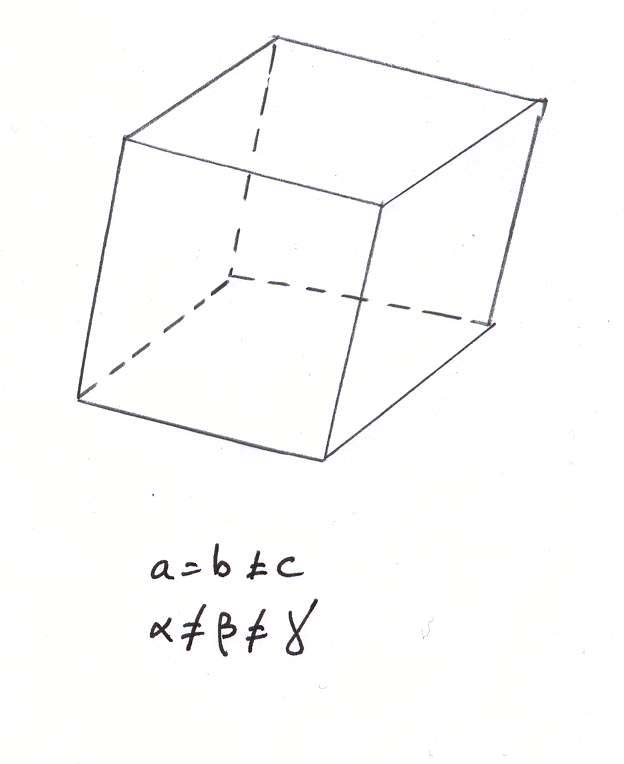
-le système orthorhombique :
La maille élémentaire est prisme droit dont la base est un losange. L’olivine, la baryte et la topaze appartiennent au système orthorhombique.
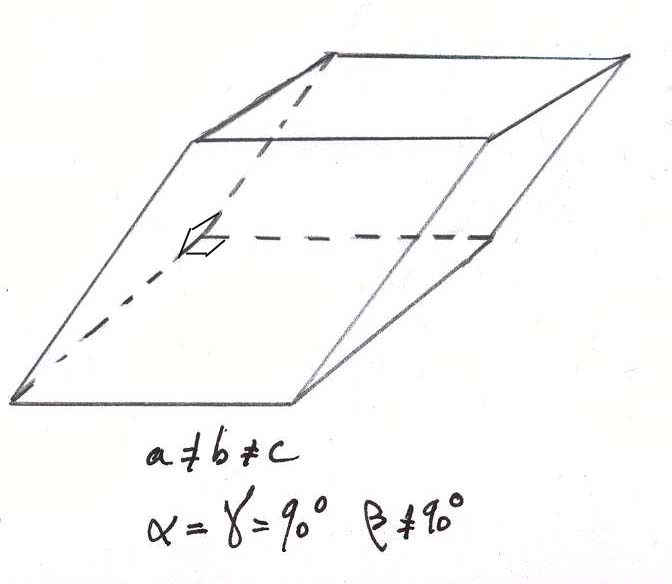
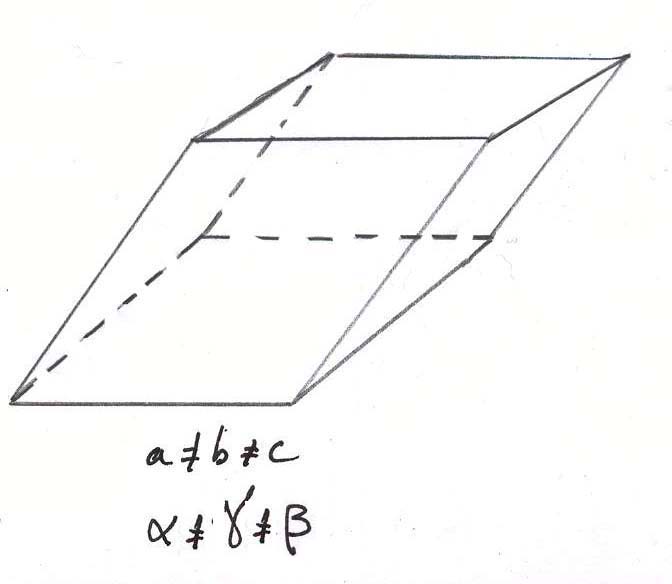
-le système monoclinique :
La maille élémentaire est un prisme droit dont la base est un parallélogramme. Ce système cristallin, le plus fréquent, comprend le gypse, l’azurite et l’orthose (feldspath potassique- FK)
-le système triclinique :
La maille élémentaire ne comprend aucun axe de symétrie. L’axinite et les feldspaths plagioclases (calco-sodiques) sont des minéraux tricliniques.
2) Les macles
Une macle est une association de 2 ou plusieurs cristaux de même nature, orientés différemment mais toujours suivant des règles cristallographiques rigoureuses.
Ex : macle simple de Carlsbad pour l’Orthose (F. potassique, K)
Deux cristaux ayant cristallisé tête bêche, quand on examine à la lumière naturelle, l'un brille quand l'autre devient terne et les rôles s'inversent en retournant l'échantillon

Ex : macle polysynthétique pour l’Albite (F. plagioclase, Na)
Ex : macle fer de lance ou en queue d’hirondelle pour le gypse

Ex : macle de la Gardette (référence mondiale) pour le quartz

3) La dureté
C’est la résistance d’un minéral à la destruction mécanique de sa structure ; en pratique, un minéral est dit plus dur qu’un autre, s’il raye ce dernier. Avec une pointe du minéral, on essai de rayer un objet témoin (minéral, verre, acier) après avoir pris soin d’essuyer la trace, pour s’assurer qu’il y a bien une rayure réelle, et non un effritement de la pointe. S’il y a rayure, le minéral est dit plus dur que le témoin.
On a pu ainsi établir de proche en proche, une échelle de dureté relative dont les valeurs sont proches d'une courbe de Vickers, échelle logarithmique. Les duretés sont classées par rapport à celles de 10 minéraux tests (échelle de Mohs) :
10 : diamant, 9 : corindon, 8 : topaze, 7 : quartz, (verre), 6 : feldspath orthose, (lame de couteau), 5 : apatite, 4 : fluorine, 3 : calcite, (ongle), 2 : gypse, 1 : talc
Phrase mnémotechnique de 1 à 10 : " Ton Gros Concierge Fou d’Amour Ose Quémander Tes Caresses Divines "
4) La cassure
Les plans suivant lesquels sont rangés les atomes peuvent être des plans de moindre résistance, auquel cas les cristaux se cassent suivant des faces planes appelées plans de clivages. Le mica en fournit un bon exemple : à l’aide d’un couteau ou de l’ongle, il est possible de détacher facilement des lamelles (feuillets).
5) L’éclat
Suivant que la surface brille beaucoup ou peu, l’éclat est dit métallique (ex : lame de couteau, pièce de monnaie) ou vitreux (ex : verre, porcelaine).
Tous les corps à éclat métallique sont opaques. Les corps à éclat vitreux peuvent être opaques, translucides ou transparents. On distingue comme variété de l’éclat vitreux l’éclat gras (quartz) et l’éclat vif (mica). Dans les minéraux des roches, l’éclat vitreux et ses variétés sont beaucoup plus répandus que l’éclat métallique.
6) La couleur et propriétés optiques
Elle dépend surtout de la nature chimique. Les minéraux purs ont des couleurs propres (calcite blanche, quartz transparent), mais des impuretés ou des défauts du système cristallin peuvent les modifier. La couleur n’est donc pas toujours significative.
7) La saveur
Bien laver l’échantillon avant de le goûter. Une saveur salée indique du sel gemme (halite NaCl) ou un sel de magnésium ou de potasse ; une saveur astringente, l’alun. Tous les autres minéraux et roches usuels sont insipides.
8) Action des acides
Parmi les minéraux des roches, la calcite fait effervescence avec l’acide chlorhydrique dilué à froid (contrairement à la dolomie, qui fait effervescence à HCl à chaud).
9) Caractère Hydrophile
Un matériau est dit hydrophile s’il absorbe de l’eau. Appliquer une goutte d’eau (ou salive) sur le minéral en question puis frotter avec le doigt. Le minéral est dit hydrophile si de la matière passe sur le doigt. Les argiles sont hydrophiles, humectées d’eau elles sont susceptibles d’être modelée.
10) La densité
Rapport de la masse du corps à celle d’un même volume d’eau, la densité des minéraux ou des roches peut facilement se mesurer. Elle fournit, pour la reconnaissance des roches, une donnée très utile et trop souvent négligée.
La densité moyenne des minéraux fréquemment rencontrés varie de 2,4 à 2,9.
Au-dessus, on parle de minéraux lourds (comme l’or, la magnétite ou l’hématite).
11) Action de la chaleur
Chauffé à 200°C dans un tube à essai, le gypse se transforme en plâtre, avec un dégagement d’eau qui se condense.
Chauffée vers 600°C, la calcite se transforme en chaux, avec dégagement de gaz carbonique.
12) Propriétés optiques
A l’aide du microscope polarisant, il est possible de mesurer des angles d’extinction caractéristiques de certains minéraux. Autre propriété, la biréfringence (réfraction d’un rayon lumineux en 2 directions différentes) de la calcite.
13) Mesures d’angles
Une des caractéristiques essentielles de la détermination des cristaux est la mesure des angles des faces. Ces mesures sont constantes pour les cristaux d’un même système cristallin. Les cristallographes les mesurent avec précision à l’aide d’un goniomètre
Ex : angle de la calcite 74° (rhomboèdre)
III) Les silicates
Ils représentent 95% des constituants de l’écorce terrestre. Il existe environ 600 espèces minérales de silicates.
Leur classification repose sur le mode d’assemblage des tétraèdres de (SiO4)4-
Constitués d’un atome de Silicium (Si4+) et de 4 atomes d’Oxygène (O2-)
6 cotés, 4 faces, 4 sommets
[Neso = île]
Composés de tétraèdres isolés : (SiO4)4-
Ex : péridots comme l’Olivine (vert, Orthorhombique) caractéristique des roches mantelliques : (Mg,Fe)2SiO4
Ex : Grenats (système cubique) fréquents dans roches métamorphiques
Ex : Zircon : ZrSiO4
Ex : Topaze : Al2[(F,OH)2|SiO4]
Ex : nombreux silicates d’Alumine : andalousite, silimanite, disthène, staurotide caractéristiques des roches métamorphiques (macle en croix caractéristique de la staurotide).
[Sôro = groupe]
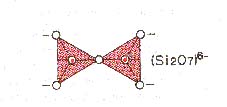
Caractérisés par des groupes de 2 tétraèdres unis par un oxygène commun : (Si2O7)6-
Assez rares. Ce sont les épidotes. Ils résultent de l'altération d'autres minéraux comme les amphiboles.
Ex : Les épidotes colorées en vert dans les schistes (métamorphisme faible) sont généralement monocliniques : OH.Ca2(AlFe)3(SiO4)3
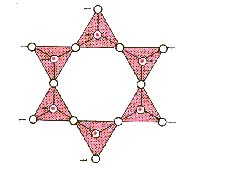
[Cyclo = anneau]
Silicates en anneau où les tétraèdres forment une chaîne fermée en étant unis par un atome d’Oxygène. Sur 4 sommets, seuls deux sont liés à d'autres tétraèdres.
Ils sont caractéristiques des pegmatites (roches magmatiques à gros cristaux). Les deux plus importants sont :
Minéraux très peu altérables résistant à plusieurs cycles sédimentaires.
Les variétés pures sont des pierres précieuses (émeraude, aigue_marine, la morganite)
[Ino = chaîne]
Sur 4 sommets, seuls deux sont liés à d'autres tétraèdres. Silicates en chaînes ouvertes de tétraèdres simples ou doubles.
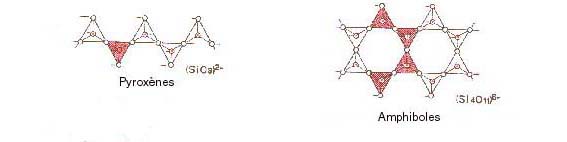
a) Les chaînes simples : les pyroxènes (px)
Ils sont caractéristiques des roches volcaniques, mais peuvent être trouvés dans des roches plus profondes basiques ou ultrabasiques (ex : enstatites (Opx), augites (Cpx))
les orthopyroxènes (Opx) :
Dans cette famille, entre les chaînes, il y a de petits ions Mg2+ et Fe2+.
C'est une série isomorphe qui s'étale entre :
- 1 pôle magnésien: Enstatite [(SI O3)2] Mg2
- 1 pôle ferreux: Orthoferrosilite. [(SI O3)2] Fe2
Les clinopyroxènes (Cpx) :
On retrouve à peu près tous les termes de la série précédente sous une forme Monoclinique, ce sont les espèces les plus nombreuses.
En plus d'être Ferromagnésien, ils sont aussi Calciques : l'Augite, noire ébène, elle est la plus fréquente dans les Basaltes et le Diopside dans les roches métamorphiques.
À ce classement nous devons ajouter des Clinopyroxènes alcalins. Ils sont de nature sodique: Na se substitue à une partie du trio [Fe, Mg, Ca] : c'est l'Aegyrine.
L'Augite aégyrinique est un minéral intermédiaire entre les 2 sous familles précédentes.
Le classement de l'ensemble des Pyroxènes s'effectue suivant le principe d'un diagramme triangulaire dont les pôles sont occupés par des minéraux contenants exclusivement soit:
- du Mg (Enstatite)
- du Fe (Ferrosilite), minéral théorique,
- du Ca (Wollastonite).
Dans une roche : on pourra trouver 1 ou 2 Pyroxènes, suivant son mode de formation.
C'est la quantité de Calcium, de plus présente, qui est le régulateur:
- si elle est faible ou nulle, on trouvera des ortho ou des Clinopyroxènes seuls;
- si elle est notable, les Orthopyroxènes coexisteront alors avec des Clinopyroxènes Calciques (mais dans ce cas, il faut, bien entendu, tenir compte du fait que d'autres minéraux, comme certains Plagioclases, se forment en utilisant aussi le Calcium).
b) Les chaînes doubles : les amphiboles
Minéraux en aiguilles. Ils ont la même chimie que les pyroxènes mais ils sont hydratés (+OH).
Dans la structure des amphiboles le couplage des chaînes fait apparaître des clivages : 2 directions faisant entre elles un angle de 122 à 126°.
On notera que la différence de valeur avec l'angle des clivages des Pyroxènes (environ 90°) est due au fait que les files d'amphiboles ont une base formée de trapèzes plus allongés que ceux des Pyroxènes.
Pôle Ca : horneblende (vert foncé)
Pôle Na : glaucophane
Pôle Fe-Mg : actinote fibreuse (un des constituant de l’amiante).
Les amphiboles peuvent provenir de la transformation des pyroxènes par ouralitisation (= auréole d’altération (amphibole) autour des pyroxène suite à l’hydratation)
Les amphiboles s’altèrent en chlorite, épidote, calcite et talc.
Pour reconnaître les cristaux de pyroxène et d'amphibole qui sont tous noirs parfois légèrement verdâtres: les amphiboles ont la forme de baguettes allongées alors que les pyroxènes sont plus des pavés proches du carré. Les cassures du pyroxène sont à 90° alors que les amphiboles présentent plutôt des clivages à 120°., les amphiboles ont une apparence plus lisses que les pyroxènes
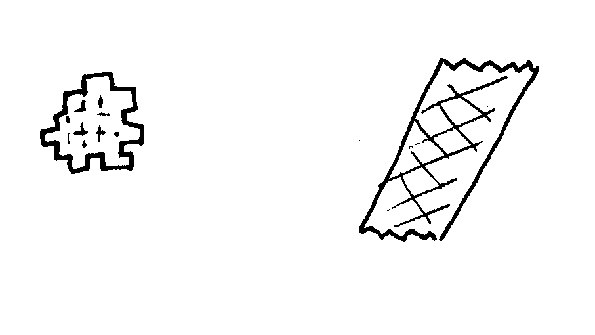
[phyllo = feuille]
Sur les 4 sommets, un seul n'est pas en relation avec un autre tétraèdre. Cette structure forme ainsi un réseau plat à maille hexagonale.
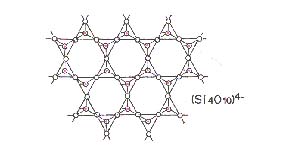
[tecto = réseau]
Chaque sommet d'un tétraèdre est en relation avec un autre tétraèdre. Les tétraèdres sont unis les uns aux autres par leurs 4 sommets
Ce sont :
-riches en potassium : orthose, sanidine (caractéristique des hautes températures) et microcline.
-ceux de la série Na-Ca : Les plagioclases. Na et Ca pouvant facilement se remplacer on trouve une série progressive de minéraux selon leur pourcentage en Na et Ca. L'albite, constitue le pôle Na, et l'anorthite le pôle Ca.
L’altération des feldspaths donne un mica blanc particulier, la séricite ou des minéraux argileux (chlorite)
Coexistence impossible entre le Quart et les Feldspathoïdes (sous-saturés)
IV) Les minéraux non-silicatés
1) Les éléments natifs
Les métalloïdes sont des éléments sont des éléments de la classification périodiques qui ne sont pas des métaux mais dont les oxydes sont acides : soufre (SO2), phosphore (PO2), carbone (CO2)…
2) les halogénures
3) les sulfures
galène (PbS),
Blende (ZnS),
Pyrite (FeS2, or des fous) et Marcassite (FeS2)
Chalcopyrite (CuFeS2)
4) les oxydes
Magnétite (Fe3O4)
Hématite (Fe2O3) noire qui laisse des traces rouge sang
Rutile (TiO2), Anatase (TiO2)
Le Corindon (Al2O3) : le saphir comme le rubis est un corindon (dureté de 9)
Dans le groupe des spinelles, on distingue le spinelle au sens strict de formule chimique MgAl2O4. Dans cette structure, le magnésium (Mg) peut être partiellement remplacé par le fer (Fe). L'aluminium (Al) peut être remplacé partiellement par du chrome (Cr). Le spinelle des lherzolites a pour formule (Mg,Fe)(Al,Cr)2O4
Remarque : la magnétite et la chromite font également partie du groupe des spinelles
5) les carbonates
6) les sulfates
7) les phosphates
EXEMPLES DE QUELQUES MINERAUX USUELS…
|
Le Quartz |
|
|
|
Le quartz est un oxyde de silicium généralement transparent ou translucide dont l'éclat peut être vitreux ou gras. Il est omniprésent à la surface de notre planète. Il est souvent grisâtre ou blanchâtre mais parfois noir, mauve bleu ou jaune. On le distingue des autres minéraux semblables par son absence de plan de cassure (clivage). En fait, lorsque l'on frappe sur le quartz, celui-ci se brise de la même façon que le verre, créant une cassure arrondie (cassure conchoïdale) évoquant l'intérieur d'une coquille. |
Le quartz possède une dureté suffisante pour rayer le verre, on lui connaît donc plusieurs utilités. Il est souvent employé comme abrasif sur les papiers sablés, il sert également pour fabriquer la céramique, la porcelaine, la vitre et les contenants de verre. Les cristaux purs et limpides ainsi que les variétés colorées servent en joaillerie. À cause de leur propriété piézo-électrique (de produire de l'électricité sous l'effet d'une pression), les cristaux de quartz sont employés dans les transmetteurs radiophoniques et les appareils électroniques de précision. Les cristaux limpides et purs sont employés en optique.
|
|
La calcite Du latin calx, calcis, qui veut dire chaux, la calcite est généralement blanche, mais peut aussi être incolore ou encore prendre des couleurs très variées. Son éclat est vitreux ou parfois mat, le plus souvent translucide elle peut aussi être transparente. Une image observée à travers un cristal de calcite se verra dédoublée. La calcite est soluble à l'acide HCl 10%, elle réagit alors avec effervescence. Elle présente également de belles faces de clivages. |
Les Feldspaths
Les feldspaths sont de loin les minéraux les plus abondants sur Terre. Ils forment un grand ensemble de minéraux que l'on divise en deux grands groupes distincts.
Les Feldspaths Plagioclases
Les feldspaths plagioclases forment une série continue de minéraux de composition chimique différente. On doit déterminer le nom d'un minéral à partir de sa chimie.
|
|
La labradorite est un feldspath plagioclase riche en calcium. Ce minéral sombre est apprécié pour ses reflets chatoyants qui vont du bleu indigo au vert turquoise en passant par toute une gamme de violets étincelants. Il possède deux clivages parfaits en plus de macles polysynthétiques (il s'agit d'un type spécial d'agencement de plusieurs cristaux en lamelles). |
|
Les feldspaths potassiques se brisent suivant deux plans de clivage bien nets. La couleur de ces minéraux est habituellement rose à orangée mais peut parfois être incolore, blanche, verte ou même rougeâtre. Ils entrent dans la fabrication des céramiques, des porcelaines, du verre, des briques, dans les savons et les poudres de récurage. |
|
|
|
Le graphite Du grec graphein qui veut dire écrire. Il est essentiellement constitué de carbone (C). D'apparence graisseuse à luisante, le graphite se présente dans Lanaudière en veines et en paillettes disséminées. Le graphite possède une vaste gamme de propriétés physiques et chimiques le rendant très convoité. |
Ce minéral gris métallique est tellement tendre qu'il tache les doigts et il constitue la mine à l'intérieur de nos crayons. Il est également souple, bon conducteur électrique, pratiquement inerte chimiquement en plus d'être difficilement fusible. On l'utilise en métallurgie, dans la fabrication des piles, batteries, céramiques, peintures anticorrosives et antistatiques, le caoutchouc, panneaux solaires, des garnitures de freins et les écrans cathodiques.
|
|
Le Grenat Du latin granatum qui signifie grenade, le fruit rouge à petits grains. Le grenat forme un groupe de plusieurs espèces se distinguant principalement par leur composition chimique et leurs couleurs. Dans Lanaudière, on retrouve souvent le grenat de couleur rouge intense et parfois d'un rose violacé. Ils forment des cristaux d'aspect granulaire dont les faces forment de petits losanges. |
Son éclat est vitreux et il réfléchit très vivement la lumière. C'est également un minéral dont la dureté élevée lui permet de rayer le verre. On utilise donc les variétés limpides de grenat en joaillerie alors que les variétés moins spectaculaires servent d'abrasifs pour le sablage à jet ou avec le papier.
|
La Biotite La biotite est un mica noir contenant du fer et du magnésium. Elle fut nommée ainsi en l'honneur du physicien français, Jean-Baptiste Biot. Comme tous les micas, la biotite possède un clivage parfait permettant de se séparer en minces feuillets. Ces feuillets transparents d'éclats vitreux, résistants, flexibles et élastiques offrent des propriétés thermiques et électriques intéressantes. |
|
On utilise la biotite dans la fabrication d'équipement électrique et électronique, des matériaux d'isolation, des peintures, des ciments et des plastiques.
Principales troncatures selon le système de cristallisation.
Cubique:
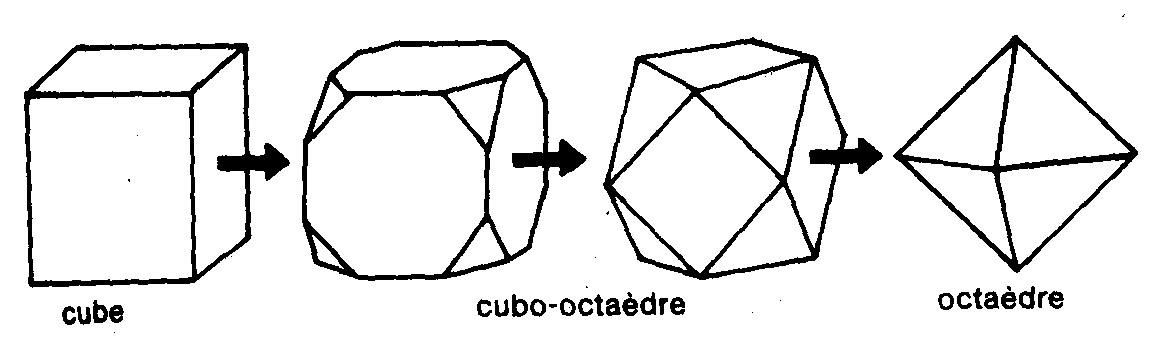
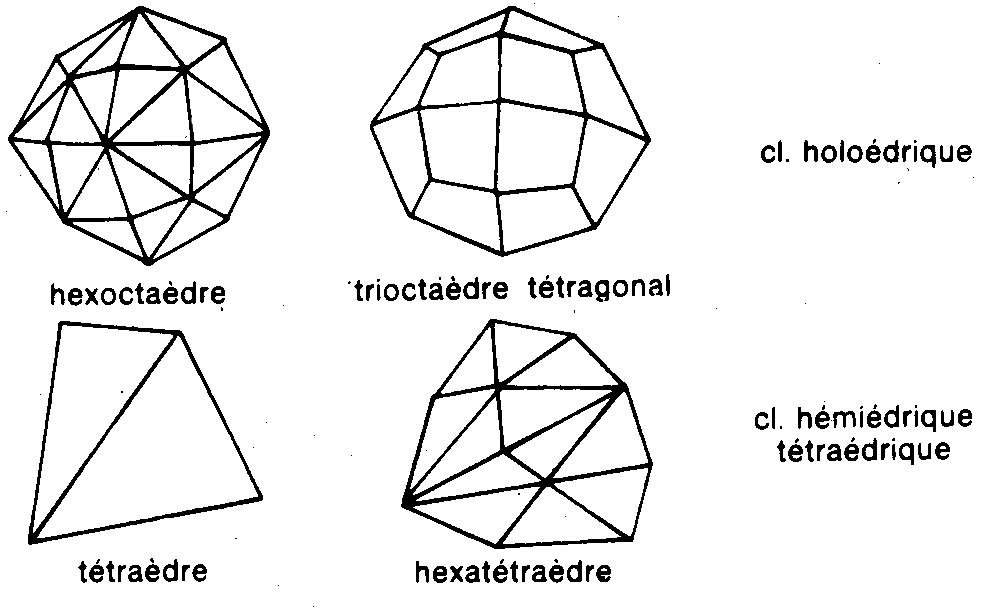
Quadratique.
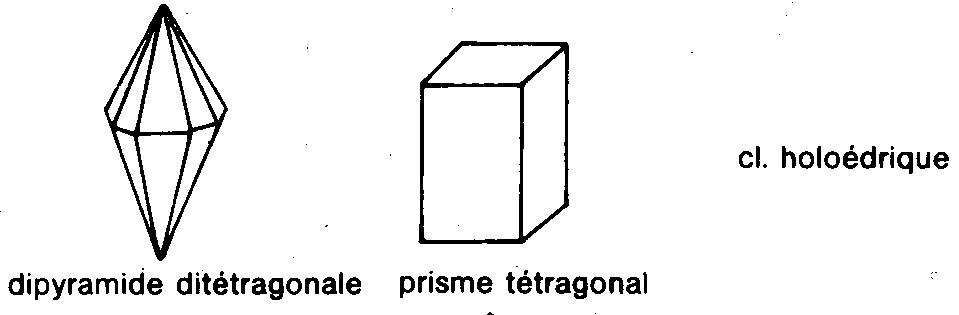
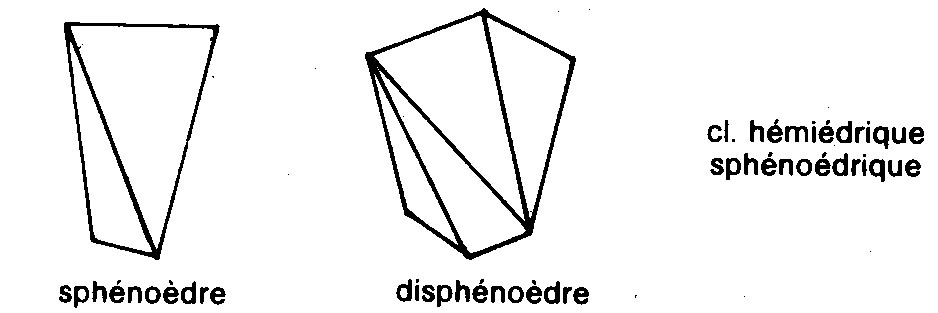
Rhomboédrique.

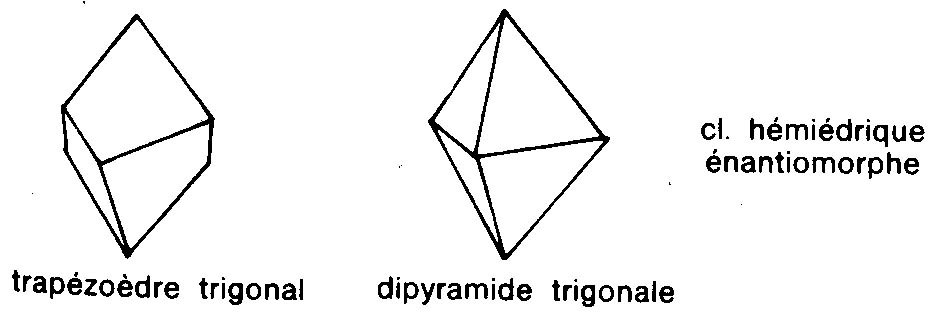
Orthorhombique.
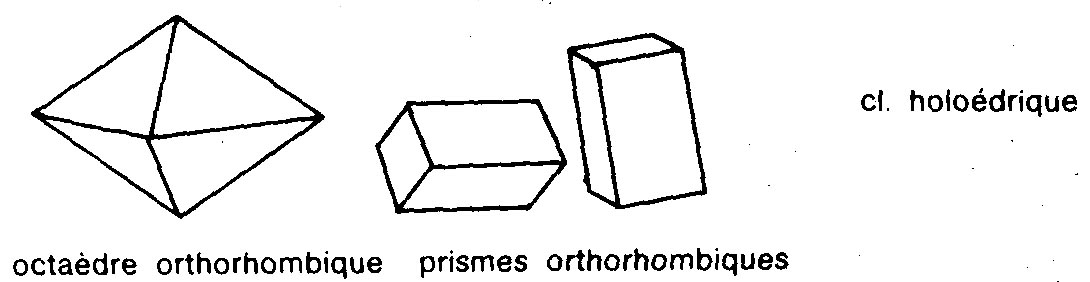
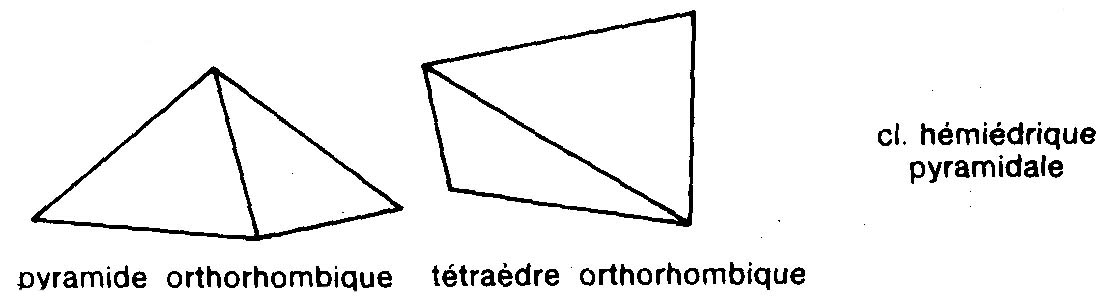
Hexagonal.